Сборник задач и упражнений по химии 8-9 классы к учебникам: Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 8 класс» и «Химия. 9 класс» - 2016 год
Соединения железа - Металлы - 9 класс
7.296. Как кислотные свойства зависят от степени окисления элемента, образующего кислоту? Какая кислота сильнее:
![]()
7.297. Как основные свойства основания зависят от степени окисления металла, образующего основания? Какой гидроксид имеет большие основные свойства:

7.298. Напишите уравнения возможных реакций:
![]()
7.299. Напишите уравнения возможных реакций:
![]()
7.300. Напишите уравнения возможных реакций:

Какая реакция является окислительно-восстановительной?
7.301. Напишите уравнения возможных реакций:
![]()
7.302. Какой цвет имеет осадок Fe(OH)2? Как этот цвет меняется под действием кислорода воздуха? Как можно отличить осадок Fe(OH)3от осадка Fe(OH)2?
7.303. Напишите уравнения следующих реакций в молекулярном и ионном виде:
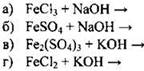
7.304. Напишите уравнение гидролиза хлорида железа(Ш) в молекулярной и ионной форме. Добавление какого из нижеперечисленных веществ уменьшает гидролиз хлорида железа(III):
![]()
7.305. Какую среду имеют растворы следующих солей:
![]()
Какую окраску имеют в этих растворах индикаторы:
а) метилоранж, .
б) лакмус,
в) фенолфталеин?
7.306. Напишите уравнения реакций следующих превращений:

7.307. Поставьте коэффициенты в уравнениях реакций, укажите окислитель и восстановитель:

7.308. Поставьте коэффициенты в уравнениях реакций, укажите окислитель и восстановитель:

7.309. Расскажите, как, имея три раствора — NaOH, AgNO3 и ВаСl2, можно различить следующие растворы:
![]()
Напишите уравнения необходимых реакций в молекулярной и ионной форме.
7.310. При обжиге минерала пирита, содержащего 90% FeS2, получено 22,4 л оксида серы(IV). Определите:
а) массу израсходованного пирита,
б) массу образовавшегося оксида железа(III).
7.311. Оксид железа(III) массой 48 г обработали избытком соляной кислоты. Определите:
а) массу образовавшейся соли,
б) массу вступившего в реакцию хлороводорода.
7.312. Смесь металлического железа и оксида железа(II) обработали избытком соляной кислоты. Определите массовую долю оксида железа(II) в исходной смеси, если в ходе реакции образовалось 63,5 г соли и выделилось 6,72 л (н.у.) газа.
7.313. Смесь оксида железа(II) и оксида железа(III) массой 60,8 г обработали избытком соляной кислоты. Определите массовую долю оксида железа(II) в исходной смеси, если в ходе реакции образовалось 115,8 г смеси солей.
7.314. К раствору хлорида железа(III) с массовой долей 0,12 прибавили избыток раствора гидроксида натрия. Определите:
а) массу исходного раствора хлорида железа(III), если в ходе реакции образовалось 42,8 г красно-бурого осадка,
б) массу вступившего при этом в реакцию гидроксида натрия.
7.315. К 89,1 мл 16%-ного раствора хлорида железа(III) с плотностью 1,14 г/мл прибавили 255,2 мл 12% раствора нитрата серебра с плотностью 1,11 г/мл. Определите массу образовавшегося осадка.
7.316. Укажите соединение железа, в котором степень окисления железа равна +2.
![]()
7.317. Поставьте коэффициенты в уравнении реакции: ![]() Ответ дайте в виде коэффициента перед восстановителем.
Ответ дайте в виде коэффициента перед восстановителем.
1) 1
2) 2
3) 3
4) 4
7.318. Сокращенному ионному уравнению: ![]() соответствует взаимодействие следующих веществ
соответствует взаимодействие следующих веществ
![]()
7.319. Сокращенному ионному уравнению: ![]() соответствует взаимодействие следующих веществ
соответствует взаимодействие следующих веществ
![]()
7.320. Укажите верное суждение:
а) гидроксид железа(III) является более сильным основанием, чем гидроксид железа(II);
б) гидроксид железа(III) имеет амфотерные свойства в отличие от гидроксида железа(II).
1) верно только а.
2) верно только б
3) верны оба суждени.
4) оба суждения неверны
7.321. Укажите вещество, с раствором которого взаимодействует гидроксид железа(II).
![]()
7.322. Определите вещества X и Y в следующей схеме превращений:
![]()
![]()
7.323. Определите вещества X и Y в следующей схеме превращений:
![]()
![]()
7.324. Определите вещество Y в следующей схеме превращений:
![]()
![]()
7.325. Определите вещество Y в следующей схеме превращений:
![]()
![]()