Сборник задач и упражнений по химии 8-9 классы к учебникам: Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 8 класс» и «Химия. 9 класс» - 2016 год
Оксиды - Важнейшие классы неорганических соединений - 8 класс
6.1. Напишите формулы следующих оксидов:
а) оксид железа(III),.
б) оксид марганца(II),
в) оксид натрия, .
г) оксид цинка,
д) оксид алюминия,.
е) оксид хрома(VI),
ж) оксид магния, .
з) оксид марганца(VII).
6.2. Назовите следующие оксиды:

6.3. Укажите основные оксиды:

6.4. Укажите кислотные оксиды:

6.5. Напишите уравнения реакций получения оксидов из простых веществ по схемам:

6.6. Напишите уравнения реакций получения оксидов окислением сложных веществ по схемам:
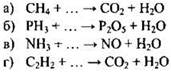
6.7. Напишите уравнения реакций получения оксидов при разложении сложных веществ по схемам:

6.8. Укажите растворимые в воде оксиды:

6.9. Напишите уравнение реакции основного оксида с водой, если такая реакция идет.

6.10. Напишите уравнение реакции кислотного оксида с водой, если такая реакция идет.

6.11. Напишите уравнение реакции основного оксида с кислотой,
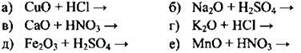
6.12. Напишите уравнение реакции кислотного оксида с щелочью,

6.13. Определите массовую долю хрома в следующем оксиде:
а) СrO, .
б) Сг2O3, .
в) СrO3.
6.14. Выведите химическую формулу оксида марганца, если массовая доля марганца в оксиде равна:
а) 0,775, .
б) 0,632,
в) 0,534, .
г) 0,495.
6.15. Определите массу оксида меди(II), образующегося при термическом разложении:
а) 19,6 г гидроксида меди(II),
б) 2,5 моль гидроксида меди(II).
6.16. Определите массу оксида кальция, образующегося при термическом разложении:
а) 20 г карбоната кальция,
б) 3,5 моль карбоната кальция.
6.17. Определите массу гидроксида натрия, образующегося при растворении в избытке воды:
а) 3,1 г оксида натрия,
б) 2,5 моль оксида натрия.
6.18. Определите массу серной кислоты, образующейся при растворении в избытке воды:
а) 2,5 моль оксида серы(VI),
б) 16 г оксида серы(VI).
6.19. Определите массу сульфата меди(II), образующегося при растворении в избытке серной кислоты:
а) 32 г оксида меди(II),
б) 3,5 моль оксида меди(II).
6.20. Определите массу сульфата натрия, образующегося при растворении в избытке гидроксида натрия:
а) 1,5 моль оксида серы(VI),
б) 48 г оксида серы(VI).
6.21. Формула оксида алюминия
1) Аl2O .
2) АlO
3) Аl2O3 .
4) АlO2
6.22. Формула оксида марганца(УИ)
1) Мn2O3 .
2) Мn2O7
3) МnO3 .
4) МnO7
6.23. Назовите оксид СuО
1) оксид меди .
2) оксид меди(I)
3) оксид меди(III) .
4) оксид меди(II)
6.24. Назовите оксид SO2
1) оксид серы(IV)
3) оксид серы(VI)
2) оксид серы(II)
4) оксид серы(II)
6.25. Укажите формулу основного оксида
1) SO2 .
2) СrO3
3) К2O .
4) Р2O5
6.26. Укажите формулу кислотного оксида
1) МnО .
2) Мn2O7
3) Na2O .
4) CuO
6.27. Укажите формулу гидроксида, который соответствует оксиду SO2
1) H2SO3 .
2) H2S
3) H2S2O7 .
4) H2SO4
6.28. Укажите формулу оксида, которому соответствует серная кислота H2SO4
1) SO .
2) SO2
3) SO3 .
4) SO4
6.29. Два элемента, которые образуют как основные, так и кислотные оксиды
1) Mg и Мn .
2) Сr и Са
3) S и P .
4) Сr и МN
6.30. Основным и кислотным оксидом являются соответственно
![]()
6.31. Кислотный оксид, который образуется при разложении сернистой кислоты H2SO3
1) SO .
2) SO2
3) SO3 .
4) SO4
6.32. Основный оксид, который образуется при разложении СаСO3
1) СO3 .
2) СO2
3) СаО .
4) СаO2
6.33. Оксид, который образуется при горении на воздухе серы
1) SO .
2) SO2
3) SO3 .
4) SO4
6.34. Оксид, который образуется при горении на воздухе фосфора
1) РО .
2) Р2O3
3) РO2 .
4) Р2O5
6.35. Укажите основный оксид, который не растворяется в воде
1) СuО .
2) Na2O
3) SiO2 .
4) CaO
6.36. Укажите кислотный оксид, который не растворяется в воде
1) Fe2O3 .
2) СrO3
3) Мn2O7 .
4) SiO2
6.37. При взаимодействии оксида серы(IV) SO2 с гидроксидом натрия NaOH образуется соль, формула которой
1) Na2SO3 .
2) NaSO3
3) Na2SO4 .
4) NaSO4
6.38. Определите массовую долю серы в оксиде серы(VI)
1) 0,60 .
2) 0,50
3) 0,40 .
4) 0,30
6.39. Укажите вещество X в следующей схеме превращений: ![]()
1) РН3 .
2) Р2O5
3) Р2O3 .
4) НРО3
6.40. Укажите вещество X в следующей схеме превращений: ![]()
1) Сu2O .
2) Сu(ОН)2
3) СuОН .
4) СuО