Сборник задач и упражнений по химии 8-9 классы к учебникам: Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 8 класс» и «Химия. 9 класс» - 2016 год
Химические свойства солей - Важнейшие классы неорганических соединений - 8 класс
6.186. Напишите по два уравнения получения следующих солей:
а) сульфата железа(II),
б) хлорида лития,
в) сульфата цинка.
г) хлорида алюминия,
д) сульфата натрия.
е) хлорида кальция.
Укажите типы химических реакций.
6.187. Какие основания могут вступать в реакции с солями? Укажите условия взаимодействия оснований с солями. Напишите уравнения осуществимых реакций по схемам:
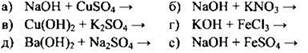
6.188. Укажите условия взаимодействия солей с кислотами и солями. Напишите уравнения осуществимых реакций по схемам:

6.189. Закончите уравнения реакций. Поставьте коэффициенты.

6.190. Закончите уравнения реакций. Поставьте коэффициенты.

6.191. Определите формулу соли, которая содержит по массе:
а) 47,4% меди и 52,6% хлора,
б) 34,5% железа и 65,5% хлора.
6.192. Определите формулу соли, которая содержит по массе:
а) 40,0% кальция, 12,0% углерода и 48,0% кислорода,
б) 23,1% железа, 17,4% азота и 59,5% кислорода.
6.193. Напишите уравнения реакций взаимодействия 1 моль Аl(ОН)3:
а) с 3 моль НСl,
б) с 2 моль НСl,
в) с 1 моль НСl.
Назовите образовавшиеся соли.
6.194. Напишите уравнения реакций взаимодействия 1 моль Н3РО4:
а) с 3 моль NaOH,
б) с 2 моль NaOH,
в) с 1 моль NaOH.
Назовите образовавшиеся соли.
6.195. Укажите, с какими из нижеперечисленных веществ будет взаимодействовать в водном растворе сульфат меди(II):
а) соляная кислота.
б) гидроксид натрия,
в) хлорид бария,.
г) железо,
д) гидроксид цинка.
е) серебро,
ж) сульфид натрия.
з) хлорид серебра(I).
6.196. Напишите уравнения реакций по следующим схемам:

6.197. Определите массовую долю фосфора в следующих веществах:

6.198. Оксид алюминия массой 30,6 г прореагировал с избытком серной кислоты. Определите:
а) массу образовавшейся соли,
б) массу прореагировавшей серной кислоты,
в) количество вещества образовавшейся воды.
6.199. Оксид меди(II) массой 32,0 г прореагировал с избытком соляной кислоты. Определите:
а) количество вещества прореагировавшего хлороводорода НСl,
б) массу образовавшейся соли,
в) массу образовавшейся воды.
6.200. Раствор хлорида кальция взаимодействует с раствором карбоната натрия. Определите:
а) массу осадка, образовавшегося из 0,3 моль хлорида кальция,
б) массу карбоната натрия, необходимую для получения 0,8 моль хлорида натрия,
в) массу осадка, образующегося при получении 81,9 г хлорида натрия,
г) массу карбоната натрия, необходимую для реакции с 55,5 г хлорида кальция.
6.201. Укажите вещество X в следующей схеме превращений: ![]()
1) MgCO3
2) Mg
3) MgO
4) Mg(OH)2
6.202. Укажите вещество X в следующей схеме превращений: ![]()
1) Са
2) СаО
3) Са(ОН)2
4) СаСl2
6.203. Укажите вещество X в следующей схеме превращений: ![]()
1) H2SO3.
2) H2SO4
3) SO2 .
4) SO3
6.204. Соль не образуется при взаимодействии
1) металла с кислотой
2) основного оксида с кислотой
3) кислотного оксида с щелочью
4) кислотного оксида с кислотой
6.205. Соль не образуется при взаимодействии
1) основания с кислотой
2) основного оксида с кислотой
3) основного оксида с основанием
4) двух солей
6.206. Раствор сульфата меди(II) не реагирует с
1) магнием .
2) ртутью
3) железом .
4) цинком
6.207. Металлическое железо реагирует с раствором следующей соли
1) SnCl2 .
2) ZnCl2
3) MgCl2 .
4) NaCl
6.208. Раствор угольной кислоты реагирует с раствором следующей соли
1) NaCl .
2) NaNO3
3) Na2SO4 .
4) Na2SiO3
6.209. Раствор гидроксида натрия реагирует с раствором следующей соли
1) Ba(NO3)2 .
2) FeCl3
3) К3РO4 .
4) Са3(РO4)2
6.210. Укажите две соли, которые реагируют друг с другом в водном растворе
