Сборник задач и упражнений по химии 8-9 классы к учебникам: Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 8 класс» и «Химия. 9 класс» - 2016 год
Оксид серы(VI). Серная кислота - Кислород и сера - 9 класс
4.121. Расскажите о физических свойствах оксида серы(VI) SO3. Напишите уравнение реакции серного ангидрида с водой.
4.122. Изобразите структурную формулу серной кислоты. Укажите валентности серы, кислорода и водорода в молекуле серной кислоты.
4.123. Определите степень окисления серы в молекулах SO3 и H2SO4. Укажите, является ли эта степень окисления для серы высшей, низшей или промежуточной. Какие свойства, окислительные или восстановительные, характерны для этих соединений?
4.124. Укажите, какую окраску имеют в разбавленном растворе серной кислоты следующие индикаторы:
а) метилоранж,
б) лакмус,
в) фенолфталеин.
4.125. Как можно разбавить концентрированную серную кислоту?
4.126. Перечислите три стадии получения серной кислоты в промышленности.
4.127. Какая первая стадия получения серной кислоты в промышленности? Напишите уравнения реакций получения оксида серы(IV) окислением следующих веществ:
а) S,
б) FeS2,
в) ZnS,
г) H2S,
д) Cu2S.
4.128. Для реакции горения серы: ![]() определите:
определите:
а) объем SO2 (н.у.), образующегося при сгорании 16 г серы;
б) объем кислорода (н.у.), необходимого для получения 16 г SO2;
в) массу серы, необходимой для получения 112 л (н.у.) SO2;
г) объем воздуха (н.у.), необходимого для полного сгорания 24 г серы, если объемная доля кислорода в воздухе равна 0,21.
4.129. Определите объем (н.у.) оксида серы(IV), который образуется при обжиге:
а) 60 г FeS2,
б) 19,2 г CuS.
4.130. Определите массовую долю FeS2 в пирите, если при обжиге:
а) 3,0 кг пирита было получено 896 л (н.у.) оксида серы(IV),
б) 100 г пирита было получено 33,6 л (н.у.) оксида серы(IV).
4.131. Для реакции горения сероводорода ![]()
![]() определите:
определите:
а) массу паров воды, образующихся при сгорании 4 моль сероводорода;
б) объем (н.у.) кислорода, необходимого для получения 3 моль оксида серы(IV);
в) массу сероводорода, для сжигания которого необходимо 48 г кислорода;
г) объем воздуха (н.у.), необходимого для полного сгорания 17 г сероводорода, если объемная доля кислорода в воздухе равна 0,21.
4.132. Для реакции ![]() определите
определите
а) массу оксида серы(VI), образующегося при окислении 32 г оксида серы(IV);
б) объем (н.у.) оксида серы(IV), необходимого для получения 20 г оксида серы(VI);
в) объем (н.у.) кислорода, необходимого для окисления 5 моль оксида серы(IV).
4.133. Определите массу 80%-ного раствора серной кислоты, которую можно получить:
а) из 320 г серы,.
б) из 20 г S03.
4.134. Определите массу серной кислоты, которую можно получить:
а) из 320 г пирита, содержащего 75% FeS2,
б) из 600 г пирита, содержащего 80% FeS2.
4.135. Определите массу пирита, содержащего 80% FeS2, необходимую для получения:.
а) 500 г 98%-ного раствора серной кислоты,
б) 272,2 г 90%-ного раствора серной кислоты.
4.136. Как разбавленная серная кислота реагирует с металлами? Напишите уравнения следующих реакций, указав, какие из них не идут:

4.137. Как концентрированная серная кислота реагирует с металлами? Какие металлы пассивируются концентрированной серной кислотой? Напишите уравнения следующих реакций, указав, какие из них не идут:
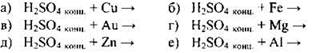
4.138. С какими оксидами реагирует в водном растворе серная кислота? Укажите, с какими из ниже перечисленных оксидов будет реагировать серная кислота:

4.139. Напишите уравнения следующих реакций в растворе, указав, какие из них не идут:

4.140. Как называют реакцию кислоты с основанием? Напишите молекулярные и ионные уравнения следующих реакций серной кислоты с основаниями:

4.141. Укажите условие взаимодействия разбавленной серной кислоты с растворами солей. Напишите молекулярные и ионные уравнения следующих реакций серной кислоты с солями, указав, какие из них не идут:

4.142. С помощью какого реактива можно обнаружить присутствие в растворе серной кислоты или сульфат-ионов? Укажите признаки этой реакции. Напишите молекулярные и ионные уравнения следующих реакций:

4.143. Установите формулу соли, содержащей:
а) 40% меди, 20% серы, 40% кислорода,
б) 46,7% железа и 53,3% серы,
в) 36,5% натрия, 25,4% серы и 38,1% кислорода,
г) 36% алюминия и 64% серы.
4.144. Определите объем водорода (н.у.), который выделяется при растворении в избытке разбавленной серной кислоты:
а) 6,0 г магния, .
б) 26 г цинка,
в) 27 г алюминия,.
г) 28 г железа.
4.145. Определите объем раствора серной кислоты с массовой долей 0,12 и плотностью 1,08 г/мл, необходимый для растворения:
а) 10,8 г алюминия.
б) 9,6 г магния,
в) 11,2 г железа,.
г) 32,5 г цинка.
4.146. Определите массу средней соли, образующейся при растворении в серной кислоте:
а) 22,4 г оксида кальция.
б) 10 г оксида магния,
в) 32 г оксида меди(II),
г) 51 г оксида алюминия.
4.147. Определите массу раствора серной кислоты с массовой долей 0,245, необходимую для растворения:
а) 8,1 г оксида цинка.
б) 3,6 г оксида железа(II),
в) 12 г оксида меди(II),.
г) 7,75 г оксида натрия.
4.148. Определите объем газа (н.у.), который выделяется при взаимодействии избытка серной кислоты:
а) с 31,8 г карбоната натрия,
б) с 22 г сульфида калия.
4.149. Определите массу осадка, образующего при взаимодействии в растворе:
а) 0,2 моль H2SO4 и 0,3 моль ВаСl2,
б) 19,6 г H2SO4 и 20,8 г ВаСl2.
4.150. К 137 мл раствора сульфата натрия с массовой долей 0,12 и плотностью 1,11 г/мл прилили 292 мл раствора хлорида бария с массовой долей 0,08 и плотностью 1,08 г/мл. Определите массу образовавшегося осадка.
4.151. Укажите характеристики, относящиеся к серному ангидриду:
а) бесцветный газ при комнатной температуре,
б) маслянистая жидкость при комнатной температуре,
в) кислотный оксид,
г) основный оксид,
д) растворим в воде с поглощением теплоты,
е) имеет молекулярную кристаллическую решетку.
1) а, в, е
2) б, в, д
3) б, в, е
4) б, д, е
4.152. Соединения серы в степени окисления +6 могут иметь свойства
1) только восстановительные
2) только окислительные
3) и окислительные, и восстановительные
4) не имеют подобных свойств
4.153. Валентность и степень окисления серы в серной кислоте равны соответственно
1) VI и +6 .
2) IV и +6
3) VI и +4 .
4) II и -2
4.154. Степень окисления серы в основном компоненте минерала пирита — FeS2 равна
1) -2.
2) -1.
3) 0 .
4) +1
4.155. Вторая стадия получения серной кислоты трехстадийным контактным способом описывается уравнением реакции

4.156. При горении серы образуется преимущественно оксид серы(IV), а оксид серы(VI) практически не образуется. Какой катализатор можно использовать для окисления оксида серы(IV) до оксида серы(VI)?
1) Fe .
2) Ni
3) MnO2 .
4) V2O5
4.157. Третья стадия получения серной кислоты трехстадийным контактным способом описывается уравнением реакции

4.158. Олеум — это раствор
1) SO3 в воде
2) SO2 в воде
3) SO3 в 100%-ной H2SO4
4) SO2 в 100%-ной H2SO4
4.159. Укажите характеристики, относящиеся к серной кислоте:
а) жидкость желтого цвета тяжелее воды,
б) бесцветная жидкость тяжелее воды,
в) сильный электролит,
г) слабый электролит,
д) бесцветная жидкость легче воды,
е) реагирует с водой с выделением теплоты,
ж) реагирует с водой с поглощением теплоты.
1) а, в, е .
2) б, в, е
з) б, г, е .
4) б, в, ж
4.160. При разбавлении концентрированной серной кислоты водой следует
1) быстро наливать кислоту в воду
2) быстро наливать воду в кислоту
3) постепенно при перемешивании наливать кислоту в воду
4) постепенно при перемешивании наливать воду в кислоту
4.161. В растворе серной кислоты лакмус имеет окраску
1) фиолетовую
2) красную
3) синюю
4) желтую
4.162. Разбавленный раствор серной кислоты не реагирует с металлом
1) железом .
2) алюминием
3) медью .
4) магнием
4.163. Раствор серной кислоты не реагирует с оксидом
![]()
4.164. Сокращенное ионное уравнение ![]() соответствует взаимодействию раствора серной кислоты с
соответствует взаимодействию раствора серной кислоты с
![]()
4.165. Разбавленная серная кислота реагирует с раствором соли
![]()
4.166. Обнаружить присутствие сульфат-ионов в растворе можно с помощью раствора, содержащего ионы
1) Fe3+ .
2) Mg2+
3) Ва2+ .
4) Cu2+
4.167. Концентрированная серная кислота растворяет медь с образованием сульфата меди(II), воды и следующего продукта
1) Н2 .
2) H2S
3) S
4) SO2
4.168. Методом электронного баланса поставьте коэффициенты в уравнении реакции:
![]()
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 18 .
2) 17
3) 16 .
4) 15
4.169. При взаимодействии в растворе одного моля серной кислоты с одним молем гидроксида натрия образуется соль
1) сульфат натрия
2) сульфит натрия
3) гидросульфат натрия
4) гидросульфит натрия
4.170. Медным купоросом называют
